Introducción
La coagulación intravascular diseminada (CID) es un síndrome adquirido, secundario a patologías subyacentes, donde la activación localizada de la coagulación y la respuesta inflamatoria generalizada, pueden llevar a daños tisulares y microvasculares donde la isquemia no es fácilmente identificable por métodos clínicos habituales o por mediciones de laboratorio simples, sin embargo se puede manifestar con falla renal, hepática, respiratoria o alteraciones del sistema nervioso central1-3.
Se conoce que esta entidad clínica se deriva, principalmente de estados infecciosos, desarrollándose en el 25 al 50% de los pacientes con sepsis de acuerdo con estadísticas a nivel mundial, aunque también se ha reportado su presencia en enfermedad hepática, neoplasias, trauma, y eventos inmunes4. A pesar de su importancia clínica, existen pocos estudios sobre el tema en los países en vías de desarrollo.
En un estudio realizado durante 7 años en la Clínica Mayo de Minnesota (Estados Unidos), se reportó que a mayor edad se incrementa la incidencia de CID en pacientes críticos, llegando a alcanzar una incidencia de más de 100 casos por 100.000 habitantes por año en hombres mayores de 80 años; respecto a la mortalidad, varía dependiendo de la ubicación geográfica y hospitalaria, la edad del paciente, los criterios diagnósticos y la causa del trastorno hemostático, reportando una mortalidad entre un 22 y 46%5,6.
Esta revisión pretende recopilar de la literatura los elementos más destacados de la CID, que permitan conocer y abordar esta complicación desde aspectos fisiopatológicos, clínicos y etiológicos, teniendo en cuenta las investigaciones actuales sobre la enfermedad y los aspectos moleculares que se encuentran en estudio para mejorar la sensibilidad del diagnóstico y la efectividad del tratamiento.
Materiales y métodos
Se realizó un estudio de revisión de la literatura sobre CID durante el año 2017 por medio de la búsqueda de artículos originales, reportes y series de casos, revisiones sistemáticas y narrativas, en las bases de datos de ciencias de la salud PubMed y ScienceDirect y en el buscador Google Scholar. Se incluyeron artículos disponibles bajo las licencias otorgadas por la Universidad Pontificia Bolivariana. Se seleccionaron en total 80 artículos, de los cuales sólo se incluyeron 51 porque la información no daba respuesta al objetivo planteado, a partir de estos se hizo la descripción del presente texto en el que se desarrolla aspectos relacionados con la Coagulación Extravascular Diseminada como tratamiento, etiología, presentación clínica y diagnóstico. Durante la búsqueda se incluyeron artículos en los idiomas español, inglés y francés. Se favoreció en la búsqueda los artículos con una fecha de publicación menor o igual a 5 años. Las principales palabras de búsqueda en español fueron coagulación intravascular diseminada, sepsis, anticoagulantes. Las principales palabras de búsqueda en inglés fueron disseminated intravascular coagulation, sepsis, anticoagulants.
Fisiopatología
De acuerdo con el Comité Científico y de Estandarización de la International Society on Thrombosis and Haemostasis (ISTH), la CID se define como un síndrome adquirido donde ocurre una activación intravascular de los sistemas de coagulación sin una localización específica, es decir, de manera sistémica, que puede resultar de diversas causas3, 7. Aunque representa del 9 al 19% de las admisiones a las Unidades de Cuidados Intensivos (UCI), los estudios sobre la incidencia general de esta complicación son limitados5.
Aunque su fisiopatología no está completamente esclarecida, la CID se relaciona con el aumento de la liberación de factor tisular (TF) y la disminución de los sistemas fibrinolíticos, existiendo una relación con acúmulos de fibrina y desgaste de los sistemas anticoagulantes endógenos8,9.
El endotelio es el órgano más importante en la patogénesis de la CID, ya que es el puente entre la lesión tisular y los componentes plasmáticos; es el sitio donde se encuentran los mecanismos hemostáticos: coagulación, anticoagulación, fibrinólisis y la antifibrinólisis; y es el encuentro de estos mecanismos, junto con las diferentes reacciones de la respuesta inflamatoria, generando daños microvasculares en componentes endoteliales como el glicocálix y otras proteínas intra y extracelulares3.
El TF, presente en el subendotelio, juega un papel central en el inicio de la coagulación: normalmente no está expuesto hasta que ocurre una lesión vascular; en ausencia de esta, los monocitos e incluso las células cancerígenas, pueden expresarlo y activar la coagulación3. En la CID se produce una activación celular que genera presencia de micropartículas procoagulantes en el sistema circulatorio, que posiblemente desequilibra la llamada respuesta inmunotrombótica mediada por los neutrófilos, y que lleva a la liberación de citoquinas inflamatorias como factor de necrosis tumoral alfa (TNFα) e interleucina 12,10.
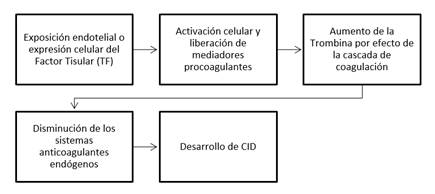
Consecuentemente, los mediadores inflamatorios y procoagulantes llevan a un aumento de la trombina, cuya función es convertir el fibrinógeno en fibrina en la última etapa de la cascada de coagulación, produciendo un aumento del gasto de los sistemas anticoagulantes del cuerpo, disminuyendo los niveles séricos de sustancias anticoagulantes endógenas como la antitrombina y la proteína C; la actividad de la antitrombina tiene un valor predictivo negativo en la CID asociada a sepsis, haciendo considerar su suplementación como alternativa de tratamiento específica para CID1,11,12. Las proteínas C y S pueden disminuir en pacientes con sepsis en consecuencia a la activación del proceso de coagulación, alteración de la síntesis hepática y degradación por la elastasa de los neutrófilos3. En la Figura 1 se esquematiza el proceso fisiopatológico de la CID
Etiología
Sepsis: Se define como una respuesta inflamatoria sistémica, ocasionada por un proceso infeccioso, que involucra daños en el endotelio vascular y genera disfunción orgánica13. Son múltiples los agentes patógenos que pueden llevar a este estado, siendo la Escherichia coli el más conocido, pero sin excluir agentes poco comunes como Acinetobacter spp. o Arthrobacter spp14-16. En la sepsis, existe una activación del sistema de coagulación mediada por la generación de trombina, que se logra evidenciar en pruebas de laboratorio como recuento plaquetario, tiempo de protrombina (TP), tiempo parcial de tromboplastina (TPT), dímero D y fibrinógeno17.
Se ha reportado una prevalencia para la CID del 10,8% en varias UCI de Colombia; su presentación en el contexto de sepsis es diferente según el tipo de infección, por ejemplo, tiene mayor incidencia en infecciones diferentes a neumonía18,19. En dos estudios realizados en Colombia, se concluyó que las bacterias Gram-Negativas son los principales agentes patógenos asociados a sepsis, seguidos por las Gram-Positivas14,20. La aparición de CID por agentes menos reportados como Plasmodium vivax hace pensar que puede estar subdiagnosticada21.
Trauma: En un trauma se presenta una respuesta inflamatoria sistémica con activación de la coagulación por la vía del TF y el factor VIIa, debido a la similitud de su presentación clínica y hallazgos con la coagulopatía aguda de trauma o shock (ACOTS, por sus siglas en inglés) pueden considerarse como una misma entidad6,22.
Neoplasias: La CID ha sido descrita en el contexto de tumores sólidos, siendo la coagulopatía más frecuente en el cáncer de próstata, además en varios tipos de leucemias, casi de manera universal como complicación de la leucemia mieloide aguda; en cualquier caso, aunque las células endoteliales también están involucradas, se cree que la CID en el contexto de las neoplasias está dada por la expresión aumentada de TF en las células cancerígenas o en los monocitos o macrófagos, activando así el proceso de la coagulación de manera difusa23,24.
Embarazo: La CID afecta a 12,5/10.000 embarazos y es la segunda causa de morbilidad materna severa en las admisiones obstétricas25. Puede resultar de complicaciones no asociadas o asociadas al embarazo entre las primeras se encuentran la sepsis o el trauma y entre las segundas están: hemorragia periparto aguda, desprendimiento placentario, preeclampsia, eclampsia, síndrome de hemólisis, elevación de enzimas hepáticas, trombocitopenia (HELLP), nacimientos muertos retenidos; aborto séptico e infección intrauterina entre otras26.
La mayoría de las CID obstétricas se deben a hemorragia masiva por lo que el tratamiento de elección inicial es controlar la hemorragia con plasma, plaquetas y crioprecipitado27. Se asocia con efectos adversos como transfusión masiva de componentes sanguíneos, histerectomía e incluso la muerte por esto es importante realizar un diagnóstico rápido y un tratamiento efectivo26.
Según el estudio realizado por Jonard et al., en mujeres embarazadas con complicaciones que requirieron ser ingresadas a UCI, llegaron a la conclusión de que los criterios diagnósticos para la CID definidos por la International Society on Thrombosis and Haemostasis (ISTH) no son recomendados para esta población debido a la baja sensibilidad, por lo que otros estudios están evaluando unos criterios que sean más acordes28.
Cuadro Clínico
Como principal causa de CID, es necesario saber identificar el cuadro clínico de la sepsis, que consiste en una respuesta anormal ante una infección, con manifestaciones como pirexia, neutrofilia y alteraciones del ritmo cardiaco, acompañados de características concretas dadas por el sitio inflamatorio y el microorganismo desencadenante29.
La presentación clínica de la CID es variada, se caracteriza por episodios trombóticos, hemorrágicos o mixtos, dependiendo en gran parte de la enfermedad de base del paciente30. Clínicamente, el componente hemorrágico se presenta como sangrado abundante o espontáneo, incluso en traumatismos leves, adicionalmente pueden encontrarse epistaxis y gingivorragias31.
El Síndrome de Disfunción Orgánica Múltiple (MODS) surge especialmente en pacientes con alto riesgo de muerte17. Este síndrome se define como una afectación de dos o más sistemas orgánicos que no estaba presente al momento de ingreso a UCI que puede ser reversible o no32. En algunos pacientes la presentación puede ser asintomática, siendo los hallazgos de laboratorio los que sugieren CID, aunque el desarrollo de tromboembolismo arterial o venoso o endocarditis no infecciosa deben ser tenidos en cuenta en el cuadro clínico24.
Diagnóstico
Actualmente existe una variedad de criterios diagnósticos para la CID, cuyo uso no está estandarizado y varía según el contexto; estos criterios incluyen los propuestos por la ISTH y la Japanese Association for Acute Medicine (JAAM), los más utilizados hoy en día en el ámbito clínico, así como otras escalas de creación reciente que buscan aumentar la especificidad y la facilidad del diagnóstico33.
La valoración propuesta por la ISHT, por ejemplo, asigna un puntaje que, de ser mayor o igual a cinco, se considera diagnóstico34; los cálculos para estas escalas tienden a basarse en pruebas de laboratorio de rutina centradas en medir el consumo de plaquetas o factores de coagulación35. En la Tabla 1 se pueden observar los criterios propuestos por la ISHT con su respectivo puntaje34. Algunos autores consideran que, no poder diagnosticar la CID en sus etapas más tempranas a partir de los criterios actuales, obligan a que estos sean reemplazados o acompañados por otras pruebas que puedan detectar y clasificar la CID incluso cuando es asintomática36.
Sin embargo, la necesidad una mayor sensibilidad al momento del diagnóstico ha llevado a la realización de múltiples estudios sobre posibles marcadores moleculares para aplicar a futuro. Un compuesto que ha demostrado ser valioso es la presepsina, un fragmento del cluster de diferenciación 14 (CD14), que da un diagnóstico más preciso al ser medido en sangre, con niveles que aumentan proporcionalmente a la severidad del cuadro clínico37. En conjunto con la proteína C se ha determinado el criterio Sepsis Induced Disseminated Intravascular Coagulation (SEDIC) aplicable a diagnóstico, clasificación de la severidad y pronóstico8.
Tabla 1. Variables utilizadas para los criterios diagnósticos para Coagulación Intravascular Diseminada de la ISHT
La formación de microtrombos por agregación plaquetaria se asocian con niveles elevados del Factor Inhibidor del Activador del Plasminógeno (PAI-1), medible por Ensayo inmunoabsorbente ligado a enzima (ELISA), y deficiencia de proteasa de escisión del factor de von Willebrand, por lo cual estos compuestos pueden ser usados como marcadores1,13. También se han considerado el componente C3 del complemento, el Complejo de Ataque de Membrana (MAC) y la Lectina de Unión a Manosa (MBL), que se encontraron elevados en pacientes sépticos con CID, al igual que los complejos monoméricos de fibrina y los productos de degradación de la misma, como el dímero D38,39. En cuanto a los complejos DNA-Histona y al DNA de doble cadena (dsDNA), resultantes del proceso de formación de Trampas Extracelulares de Neutrófilos (NETs), estos han demostrado un valor pronóstico sobre la severidad del proceso de coagulación40.
Complicaciones
El mayor riesgo de los pacientes con CID asociada a infección son los episodios trombóticos, especialmente venosos y pulmonares, también se pueden presentar eventos arteriales41. En los casos de sepsis puerperal o episodios sépticos en el embarazo, las complicaciones más importantes son la muerte materna o fetal que, en parte, pueden derivarse de la pérdida de irrigación a los órganos bien sea por oclusión o disminución del volumen sanguíneo16,42. El MODS, es una de las complicaciones más peligrosas de la CID por su elevada mortalidad17. La gangrena periférica simétrica, dada por vaso oclusión, se considera una complicación rara, pero debe ser tenida en cuenta por su gravedad, puesto que puede llevar a amputaciones43.
Tratamiento actual
Aunque la resolución del evento desencadenante o enfermedad subyacente suele ser suficiente para la corrección de la CID, el tratamiento directo de los problemas en la hemostasia permite una mejor evolución44,45. El tratamiento directo aún no está estandarizado, y varía según el país y la fuente que se consulte. En Estados Unidos, el único tratamiento aprobado hasta el año 2012 para la CID asociada a sepsis era la Proteína C activada (APC), con el uso de heparina sólo como profilaxis en pacientes sin sangrado activo41. En 2014, se reportó que la APC fue removida del mercado a causa de un estudio donde no demostró ninguna ventaja con respecto a un placebo, aunque en investigaciones previas había logrado reducir la mortalidad46.
El suplemento de los factores de coagulación y plaquetas también se ha mostrado útil gracias al uso de tecnologías modernas como la tromboelastografía para disminuir las complicaciones asociadas a transfusiones47. El tratamiento de elección a corto plazo para los pacientes con sangrado como manifestación de CID continúa siendo la terapia con componentes sanguíneos, basada en las necesidades identificadas por el clínico en las pruebas de laboratorio del paciente7.
La antitrombina (AT), un inhibidor de la trombina y el factor X, funciona como marcador de laboratorio para CID pues su consumo se asocia con la activación de la coagulación, por lo que su suplemento logra regular la alteración13. Mientras la ISTH la considera como una alternativa de tratamiento aún en investigación, la Japanese Society of Thrombosis Hemostasis y la Japanese Society of Intensive Care Medicine la recomiendan en CID derivada de sepsis, con algunos estudios demostrando efectividad11. A pesar de esto, la Italian Society for Haemostasis and Thrombosis no recomienda el uso de AT ni de trombomodulina recombinante humana (rhTM) en estos casos41. Al ser un cofactor de la heparina, su actividad se aumenta al combinarse con esta, al igual que en los estados de acidosis17. En Japón, la AT y la rhTM son la vanguardia como monoterapia del tratamiento anticoagulante en CID, pero, en combinación, se ha demostrado mayor efectividad y seguridad47.
Futuros tratamientos
En el estudio realizado por Azuma et al., observaron, que el tratamiento con la inmunoglobulina G4 recombinante anti CD33 en pacientes con leucemia promielocítica aguda (LPA), presentaban CID como principal evento adverso, pero su utilidad fue demostrada en pacientes con LPA de edad avanzada, estos pacientes fueron tratados posteriormente con rhTM para la CID48.
La rhTM actúa como anticoagulante por la vía de la proteína C activada, y está en evaluación para ser aprobada en países diferentes a Japón, aunque, como con la AT, inquieta el riesgo de sangrado49. Incluso con estas preocupaciones, estudios clínicos han indicado una disminución de la mortalidad con el uso de rhTM, con una supervivencia de 64,1% y 70,7% en los grupos estudiados50. Cuenta con propiedades antiinflamatorias al interferir con la activación del complemento, se administra intravenosa y se elimina por los riñones44. De hecho, en una investigación realizada en neonatos y comparada con pacientes adultos, se mostró mejoría en las pruebas de laboratorio con disminución en los niveles de productos de degradación de la fibrina y aumento en el conteo de plaquetas y la actividad de AT51.
Tang et al., realizaron un estudio en animales, en el que evidenciaron el papel protector del atractilenolido I que es un componente bioactivo de una planta china, sobre la CID inducida por lipopolisacáridos bacterianos, mejorando la coagulación y suprimiendo la inflamación, con la disminución de la expresión del TNFα, reduciendo el daño de órganos y aumentando la tasa de supervivencia2.
Pronóstico de los pacientes con CID
Con una mortalidad intrahospitalaria de hasta el 58% en Estados Unidos, y el alta como desenlace en sólo el 54% de los pacientes sobrevivientes, la CID es una complicación con un alto impacto en la sobrevida de los pacientes: el desenlace tiende a ser mejor si la causa subyacente es identificada y tratada de manera temprana, lo cual se hace especialmente importante por las limitadas opciones de tratamiento para la CID5. Aunque la evidencia es limitada, en los pacientes con cáncer se ha postulado que el aumento fibrinólisis promueve las metástasis, generando un pronóstico pobre23. Sin embargo, si esta complicación es manejada de manera urgente y agresiva, se puede obtener una respuesta positiva al tratamiento y prolongar la supervivencia24.
Conclusiones
El presente artículo de revisión de tema recopiló aspectos relevantes de la CID incluyendo, entre otras cosas, una breve descripción de la fisiopatología, sus principales etiologías, el diagnóstico y el tratamiento. Son diversos factores los que contribuyen al desarrollo de esta complicación y a su pronóstico, desde la patología subyacente hasta factores individuales como la edad, los cuales deben ser tenidos en cuenta para poder reconocer e identificar los casos de CID.
La CID es una complicación que contribuye a aumentar la morbilidad y la mortalidad en los pacientes con enfermedades de base. Su pronto diagnóstico y tratamiento aportan significativamente a una mejor evolución clínica, por lo cual actualmente se investigan nuevos tratamientos, así como marcadores moleculares que amplíen las posibilidades diagnósticas.
La mayor parte de los estudios, así como las guías para el diagnósticos y el tratamiento, son han sido realizados en países desarrollados como Estados Unidos, Japón e Italia, por lo que se hacen necesarios estudios que evalúen la aplicabilidad de esta información en el contexto de países como Colombia, así como estudios que permitan conocer el enfoque actual y la epidemiología de la CID en nuestro medio.